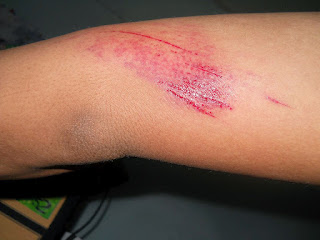
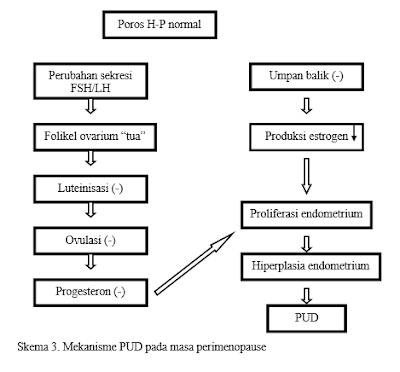
Proses penyembuhan pada luka akan melalui 3 fase yaitu :
FASE INFLAMASI
Fase ini berlangsung sejak terjadinya luka sampai kira-kira hari kelima. Pada luka akibat putusnya pembuluh darah akan terjadi perdarahan. Untuk menghentikan perdarahan ini maka akan terjadi :
Leukosit mengeluarkan enzim hidrolitik yang membantu mencerna bakteri dan kotoran luka (proses fagositosis). Pada fase selanjutnya limfosit dan monosit yang muncul dan ikut menghancurkan / memakan kotoran luka dan bakteri. Dengan fase ini maka luka hanya dipertautkan oleh fibrin sehingga perlekatan luka belum kuat.
FASE PROLIFERASI
Berlangsungnya mulai akhir fase inflamasi sampai kira-kira akhir minggu ketiga. Disebut juga fase fibroplasia karena yang menonjol adalah proses proliferasi fibroblast. Fibroblast berasal dari sel-sel mesenkim yang belum berdiferensiasi. Fibroblast ini berperan dalam pembentukan kolagen karena menghasilkan mukopolisakarida, asam aminoglisin dan prolin, yang merupakan bahan dasar kolagen. Diketahui bahwa kolagen inilah yang mempertautkan tepi luka, jadi menentukan kekuatan adhesi luka.
Pada fase ini, luka akan dipenuhi oleh sel radang, fibroblast dan kolagen, membentuk jaringan yang berwarna kemerahan dengan permukaan yang berbenjol halus / granuler, jaringan ini disebut jaringan granulasi. Jika luka sudah cukup terisi jaringan granulasi maka terjadi proses epitelisasi dimana sel epitel tepi luka yang terdiri dari sel basal terlepas dari dasarnya dan berpindah mengisi permukaan luka. Proses migrasi ini hanya boleh terjadi ke arah yang rendah atau datar. Epitel tak dapat bermigrasi ke arah yang lebih tinggi. Jika epitel sudah saling menyentuh dan menutup luka maka proses fibroplasias dengan pembentukan jaringan granulasi berhenti.
Fungsi jaringan granulasi adalah :
FASE PENYUDAHAN
Terjadi proses pematangan dan erupaan kembali (remodeling). Fase ini dapat berlangsung berbulan-bulan. Tubuh berusaha menormalkan kembali jaringan yang menjadi abnormal karena proses pertumbuhan, dimana terjadi penyerapan kembali jaringan yang berlebihan, pengerutan dan akhirnya perupaan kembali jaringan baru terbentuk.
Terjadi penyerapan dari oedem dan sel-sel radang, sel-sel muda menjadi matang, kapiler-kapiler baru menutup, kolagen yang berlebih diserap dan sisanya mengerut.
Dihasilkan jaringan parut (cicatrix) yang pucat, tipis dan lemas serta mudah digerakkan dari dasar.
KONTRAKSI LUKA
Kontraksi luka adalah suatu proses dimana terjadi penyempitan ukuran luka. Tepi-tepi luka bergerak ke arah satu terhadap lainnya membuat defek jadi lebih kecil. Ternyata luka berkontraksi dengan meregangkan kulit sekitarnya tidak dengan memproduksi kulit baru. Kontraksi ini timbul cukup awal.
Mekanisme terjadinya kontraksi ini belum diketahui dengan jelas. Pada mulanya diperkirakan terjadi akibat kontraksi kolagen. Ternyata mekanisme kontraksi lebih disebabkan oleh kontraksi fibroblast (miofibroblast). Ukuran luka dalam 10 hari bisa berkurang 80%. Dikatakan bahwa miofibroblast bekerja di balik tepi luka dan mendorong tepi-tepi luka ke arahnya.
Pada tempat-tempat tertentu di mana kulit yang mobil sangat penting maka kontraksi luka dapat mengakibatkan gangguan fungsional. Misalnya dekat mata dapat menyebabkan kelopak mata tertarik ke arah luka yang mengakibatkan kelopak mata tidak dapat menutupi bola mata dengan sempurna (ektropion) atau di punggung tangan dapat akibatkan hambatan ekstensi jari-jari.
FAKTOR-FAKTOR YANG MEMPENGARUHI PENYEMBUHAN LUKA
Ada banyak factor yang menghambat atau mengganggu penyebuhan luka, baik factor dari dalam tubuh sendiri (endogen) maupun dari luar (eksogen).
a. Faktor ENDOGEN
b. Faktor EKSOGEN
Disamping itu beberapa faktor local / setempat seperti:
KLASIFIKASI PENYEMBUHAN LUKA
Penyembuhan luka dapat berlangsung secara:
Pada manusia penyembuhan luka yang sempurna dalam arti dengan cara reorganisasi dan regenerasi jaringan hanya terjadi pada epidermis, hati dan tulang, yang artinya oleh penyembuhan terbentuk jaringan yang sama seperti semula. Organ-organ lain termasuk kulit mengalami penyembuhan secara epimorfosis artinya jaringan yang rusak diganti oleh jaringan ikat yang tidak sama dengan semula.
PENANGANAN LUKA
Penting sekali untuk evaluasi keadaan umum penderita, termasuk kemungkinan adanya cedera lain. Pada keadaan di mana keadaan umum tidak baik, penanganan luka harus ditunda, dan dilakukan tindakan-tindakan untuk memperbaiki keadaan umum, termasuk adanya ancaman langsung terhadap hidup penderita.
Terhadap luka itu sendiri maka hal yang paling penting yang dapat menjamin penyembuhan luka dengan baik adalah pembersihan luka yang baik dan benar ialah dengan membersihkan dan membuang semua kotoran dan jaringan-jaringan yang rusak / mati. Tindakan itu dikenal sebagai “debrideman”.
Harus disadari bahwa : “There is no antibiotic can substitute a good surgery”. Hal ini berarti bahwa pemakaian antibiotika tidak dapat menggantikan tindakan debrideman, bahkan dengan debrideman atau perawatan luka yang baik antibiotika mungkin tidak diperlukan.
Ada 2 tindakan pokok pada pembersihan luka yaitu :
Dengan kata lain, debrideman akan menghasilkan satu luka baru dan bersih karena yang tertinggal adalah jaringan yang sehat. Tanda dari jaringan yang sehat adalah jika dipotong menunjukkan perdarahan yang baik dan pada otot terlihat kontraksi.
Perawatan luka paling baik jika dikerjakan dalam 6 – 8 jam sesudah terjadi yang dikenal sebagai “golden period”.
Secara berurutan tindakan pada luka sebagai berikut :
Pada luka yang dalam biasanya sebaiknya dijahit lapis demi lapis, yaitu otot dengan otot, fascia dengan fascia dst. Jika diperkirakan akan terbentuk atau dikeluarkan cairan berlebihan maka dibuat penyaliran (pemasangan drain). Tapi harus diingat bahwa drain tidak dapat mengganti tindakan perawatan luka yang baik seperti hemostasis dsb.
Drain biasa dikeluarkan sesudah 48 jam, tidak boleh terlalu lama sebab drain juga merupakan benda asing, demikian pula dapat menjadi port d’entrée / pintu masuk kuman serta boleh menyebabkan erosi.
Dalam menutup luka perlu diikuti prinsip Halsted yaitu :
Sama seperti penyembuhan luka maka penutupan luka juga dikenal :
KOMPLIKASI LUKA
Penyulit dini :
Penyulit lanjut :
Perbedaan antara keloid dan parut hipertrofik :
Sebagai penutup artikel ini, telah ditemukan hal-hal yang berhubungan dengan luka dan proses penyembuhannya serta keadaan-keadaan yang mempengaruhi penyembuhan, demikian pula cara penanganannya. Diharapkan dengan dasar pengetahuan ini maka luka-luka dapat ditangani dengan baik dan benar, dengan selalu bertolak dari keyakinan bahwa : “The is no antibiotic can substitute a good surgery”.
- Fase inflamasi
- Fase proliferasi
- Fase penyudahan (remodeling
 |
| proses penyembuhan luka |
FASE INFLAMASI
Fase ini berlangsung sejak terjadinya luka sampai kira-kira hari kelima. Pada luka akibat putusnya pembuluh darah akan terjadi perdarahan. Untuk menghentikan perdarahan ini maka akan terjadi :
- Vasokonstriksi yang diakibatkan oleh lepasnya katekolamine.
- Retraksi dan hemostatis, dimana terbentuk gumpalan / bekuan darah yang dapat berfungsi sebagai penyumbat. Dalam hal ini dangat berperan adalah trombosit yang keluar dari pembuluh darah.
Leukosit mengeluarkan enzim hidrolitik yang membantu mencerna bakteri dan kotoran luka (proses fagositosis). Pada fase selanjutnya limfosit dan monosit yang muncul dan ikut menghancurkan / memakan kotoran luka dan bakteri. Dengan fase ini maka luka hanya dipertautkan oleh fibrin sehingga perlekatan luka belum kuat.
FASE PROLIFERASI
Berlangsungnya mulai akhir fase inflamasi sampai kira-kira akhir minggu ketiga. Disebut juga fase fibroplasia karena yang menonjol adalah proses proliferasi fibroblast. Fibroblast berasal dari sel-sel mesenkim yang belum berdiferensiasi. Fibroblast ini berperan dalam pembentukan kolagen karena menghasilkan mukopolisakarida, asam aminoglisin dan prolin, yang merupakan bahan dasar kolagen. Diketahui bahwa kolagen inilah yang mempertautkan tepi luka, jadi menentukan kekuatan adhesi luka.
Pada fase ini, luka akan dipenuhi oleh sel radang, fibroblast dan kolagen, membentuk jaringan yang berwarna kemerahan dengan permukaan yang berbenjol halus / granuler, jaringan ini disebut jaringan granulasi. Jika luka sudah cukup terisi jaringan granulasi maka terjadi proses epitelisasi dimana sel epitel tepi luka yang terdiri dari sel basal terlepas dari dasarnya dan berpindah mengisi permukaan luka. Proses migrasi ini hanya boleh terjadi ke arah yang rendah atau datar. Epitel tak dapat bermigrasi ke arah yang lebih tinggi. Jika epitel sudah saling menyentuh dan menutup luka maka proses fibroplasias dengan pembentukan jaringan granulasi berhenti.
Fungsi jaringan granulasi adalah :
- Mengisi defek luka
- Membentuk dasar untuk menyokong dan memberi makan pada epithelium yang meluas menutupi luka.
- Pada luka terbuka, kita dapat melihat jaringan granulasi yang sehat jika warnanya merah terang, permukaan bergranular halus teraba agak keras dan tidak mudah berdarah. Jika ada infeksi maka terdapat jaringan granulasi yang tidak sehat dimana warnanya pucat, permukaan kasar tidak teratur, lembek dan rapuh dan sangat mudah berdarah.
FASE PENYUDAHAN
Terjadi proses pematangan dan erupaan kembali (remodeling). Fase ini dapat berlangsung berbulan-bulan. Tubuh berusaha menormalkan kembali jaringan yang menjadi abnormal karena proses pertumbuhan, dimana terjadi penyerapan kembali jaringan yang berlebihan, pengerutan dan akhirnya perupaan kembali jaringan baru terbentuk.
Terjadi penyerapan dari oedem dan sel-sel radang, sel-sel muda menjadi matang, kapiler-kapiler baru menutup, kolagen yang berlebih diserap dan sisanya mengerut.
Dihasilkan jaringan parut (cicatrix) yang pucat, tipis dan lemas serta mudah digerakkan dari dasar.
KONTRAKSI LUKA
Kontraksi luka adalah suatu proses dimana terjadi penyempitan ukuran luka. Tepi-tepi luka bergerak ke arah satu terhadap lainnya membuat defek jadi lebih kecil. Ternyata luka berkontraksi dengan meregangkan kulit sekitarnya tidak dengan memproduksi kulit baru. Kontraksi ini timbul cukup awal.
Mekanisme terjadinya kontraksi ini belum diketahui dengan jelas. Pada mulanya diperkirakan terjadi akibat kontraksi kolagen. Ternyata mekanisme kontraksi lebih disebabkan oleh kontraksi fibroblast (miofibroblast). Ukuran luka dalam 10 hari bisa berkurang 80%. Dikatakan bahwa miofibroblast bekerja di balik tepi luka dan mendorong tepi-tepi luka ke arahnya.
Pada tempat-tempat tertentu di mana kulit yang mobil sangat penting maka kontraksi luka dapat mengakibatkan gangguan fungsional. Misalnya dekat mata dapat menyebabkan kelopak mata tertarik ke arah luka yang mengakibatkan kelopak mata tidak dapat menutupi bola mata dengan sempurna (ektropion) atau di punggung tangan dapat akibatkan hambatan ekstensi jari-jari.
FAKTOR-FAKTOR YANG MEMPENGARUHI PENYEMBUHAN LUKA
Ada banyak factor yang menghambat atau mengganggu penyebuhan luka, baik factor dari dalam tubuh sendiri (endogen) maupun dari luar (eksogen).
a. Faktor ENDOGEN
- Pembekuan darah. Semua penyakit yang menyebabkan gangguan pembekuan darah (koagulopati) akan menghambat penyembuhan. Diketahui bahwa homeostasis merupakan dasar dan titik tolak fase inflamasi.
- Gangguan sistim imun. Gangguan pada sistim daya tahan tubuh, seluler maupun humoral, akan mengakibatkan pembersihan kontaminan dan jaringan mati serta penanahan infeksi tidak berjalan baik. Banyak keadaan / penyakit yang mengganggu sisteim imun yaitu :
- Infeksi virus (HIV)
- Tahap lanjut dari keganasan
- Penyakit menahun berat (mis TBC)
- Hipoksia setempat (DM, arteriosclerosis, dll)
- Gizi kurang
- Kekurangan vitamin / mineral / asam amino esensial.
- Vitamin C mempunyai peranan dalam sintesa kolagen. Kekurangan kolagen mengakibatkan kekuatan adhesi luka kurang.
- Zinc. Diketahui bahwa Zinc mempengaruhi fase proliferasi terutama sel-sel epitel.
- Gangguan metabolisme makanan (mis. Penyakit hati)
- Keadaan umum kurang baik (mis. Umur lanjut)
b. Faktor EKSOGEN
- Radiasi. Menyebabkan kerusakan sel dan gangguan mitosis, juga radiasi menyebabkan fibrosis yang menghalangi vaskularisasi.
- Sitostatik. Misalnya 5F.u, MTX, yang menekan pembentukan fibroblast dan sintesa kolagen.
- Steroid. Preparat steroid menekan proses inflamasi dan meningkatkan lysys kolagen, terutama dalam 4 hari pertama.
- Imunosupresan, yaitu obat-obat yang menekan reaksi imun, seperti yang dipakai setelah transplantasi organ.
Disamping itu beberapa faktor local / setempat seperti:
- Besarnya luka.
Luka yang lebar perlu penyembuhan lama. Penjahitan luka akan mempercepat penyembuhan. Pada luka yang lebar di mana kedua tepi luka tidak dapat dirapatkan dengan penjahitan di mana epithelisasi tidak mampu untuk menutup seluruh permukaan luka disamping itu dengan kontraksi luka terjadi penyempitan pembuluh darah hingga penyembuhan terhambat, maka sering penutupan luka harus dibantu dengan grafting. - Keadaan jaringan.
Apakah dalam luka bayak kotoran / jaringan yang nekrotis. Jika banyak maka proses penyembuhan akan terhambat oleh karena itu sangat penting perawatan luka yang baik (debrideman). - Vaskularisasi setempat.
Pada tempat-tempat atau bagian tubuh dengan vaskularisasi yang baik, penyembuhan luka lebih baik seperti pada leher, wajah. Sehubungan dengan hal ini maka dalam penjahitan luka / penutupan luka jangan terlalu erat atau dipaksakan karena justru tindakan ini akan menganggu vaskularisasi dengan akibat penyembuhan luka terhambat. - Hematoma
Hematoma yang terus bertambah akan memperbesar “dead space”, dan juga dengan tekanan dalam luka yang meningkat dengan sendirinya menyebabkan gangguan vaskularisasi. Di samping itu bekuan darah menjadi medium yang baik untuk pertumbuhan kuman jadi mengundang infeksi. Oleh karena itu penting hemostasis yg baik dalam menangani luka-luka. - Benda asing / corpus alienum
Akan merangsang reaksi inflamasi yang berlebihan demikian pula proliferasi yang berlebihan hingga terbentuk kolagen yang tidak normal. - Infeksi
Jelas menghambat penyembuhan.
KLASIFIKASI PENYEMBUHAN LUKA
Penyembuhan luka dapat berlangsung secara:
- Sanatio per priman intentionem atau penyembuhan primer.
Cara penyembuhan ini terjadi pada luka insisi tanpa gap, atau bila luka segera dipertautkan dengan bantuan jahitan. Parut yang terjadi biasanya minimal / kecil dan halus. - Sanatio per secundam intentionem atau penyembuhan sekunder.
Merupakan penyembuhan luka tanpa pertolongan dari luar, yang terjadi pada luka terbuka atau tidak dijahit. Proses berjalan secara alami melalui pembentukan jaringan granulasi kemudian ditutup dengan epitel. Tentu saja cara ini memakan waktu lebih lama, dan meniggalkan parut yang tidak baik / jelek, lebih-lebih kalau lukanya menganga lebar. - Penyembuhan primer tertunda
Pada luka-luka yang sangat kotor / terkontaminasi berat atau luka compang camping atau pada luka tembak. Pada luka-luka tersebut diperkirakan akan terjadi infeksi kalau langsung dijahit. Dalam hal ini luka itu setelah dilakukan pembersihan sesuai dengan penanganan luka, tetap dibiarkan terbuka tidak dijahit. Sesudah 4 – 7 hari jika tidak terjadi infeksi baru dilakukan penjahitan.
Pada manusia penyembuhan luka yang sempurna dalam arti dengan cara reorganisasi dan regenerasi jaringan hanya terjadi pada epidermis, hati dan tulang, yang artinya oleh penyembuhan terbentuk jaringan yang sama seperti semula. Organ-organ lain termasuk kulit mengalami penyembuhan secara epimorfosis artinya jaringan yang rusak diganti oleh jaringan ikat yang tidak sama dengan semula.
PENANGANAN LUKA
Penting sekali untuk evaluasi keadaan umum penderita, termasuk kemungkinan adanya cedera lain. Pada keadaan di mana keadaan umum tidak baik, penanganan luka harus ditunda, dan dilakukan tindakan-tindakan untuk memperbaiki keadaan umum, termasuk adanya ancaman langsung terhadap hidup penderita.
Terhadap luka itu sendiri maka hal yang paling penting yang dapat menjamin penyembuhan luka dengan baik adalah pembersihan luka yang baik dan benar ialah dengan membersihkan dan membuang semua kotoran dan jaringan-jaringan yang rusak / mati. Tindakan itu dikenal sebagai “debrideman”.
Harus disadari bahwa : “There is no antibiotic can substitute a good surgery”. Hal ini berarti bahwa pemakaian antibiotika tidak dapat menggantikan tindakan debrideman, bahkan dengan debrideman atau perawatan luka yang baik antibiotika mungkin tidak diperlukan.
Ada 2 tindakan pokok pada pembersihan luka yaitu :
- Luka dicuci / dibilas dengan NaCl atau antiseptikum (dapat dipakai larutan yodium povidon 1% dan larutan klorheksidin 0,5%). Paling murah dengan air masak. Pada luka yang sangat kotor atau terkontaminasi berat dikerjakan “high pressure irrigation”.
- Eksisi jaringan yang mati atau tidak dapat bersih dengan pencucian atau jaringan yang sudah rusak sekali. Demikian pula tepi luka di eksisi supaya jadi rata.
Dengan kata lain, debrideman akan menghasilkan satu luka baru dan bersih karena yang tertinggal adalah jaringan yang sehat. Tanda dari jaringan yang sehat adalah jika dipotong menunjukkan perdarahan yang baik dan pada otot terlihat kontraksi.
Perawatan luka paling baik jika dikerjakan dalam 6 – 8 jam sesudah terjadi yang dikenal sebagai “golden period”.
Secara berurutan tindakan pada luka sebagai berikut :
- Anestesi local atau umum
- Pembilasan luka
- Sterilisasi kulit sekitar luka
- Luka dikelilingi dengan kain steril
- Pembersihan luka (debrideman) : Kotoran, Benda asing, Eksisi jaringan mati, Eksisi pinggir luka
- Hemostasis yang baik
- Kalau perlu : Ekplorasi à kerusakan tendon, saraf, pembuluh darah
- Luka sebaiknya : Ditutup pada penyembuhan primer atau biarkan terbuka pada penyembuhan primer tertunda
- Kalau perlu pemasangan penyalir (drain)
Pada luka yang dalam biasanya sebaiknya dijahit lapis demi lapis, yaitu otot dengan otot, fascia dengan fascia dst. Jika diperkirakan akan terbentuk atau dikeluarkan cairan berlebihan maka dibuat penyaliran (pemasangan drain). Tapi harus diingat bahwa drain tidak dapat mengganti tindakan perawatan luka yang baik seperti hemostasis dsb.
Drain biasa dikeluarkan sesudah 48 jam, tidak boleh terlalu lama sebab drain juga merupakan benda asing, demikian pula dapat menjadi port d’entrée / pintu masuk kuman serta boleh menyebabkan erosi.
Dalam menutup luka perlu diikuti prinsip Halsted yaitu :
- Asepsis
- Gentleness
- Hemostasis
- Adequat blood supply
- No tension
- Careful approximation
- Obliteration of dead space.
Sama seperti penyembuhan luka maka penutupan luka juga dikenal :
- Primary Suturing : penjahitan primer, dimana luka sesudah debrideman langsung dijahit / ditutup, untuk mencapai penyembuhan primer
- Delayed primary suturing : penjahitan primer tertunda dimana sesudah debrideman, luka dibiarkan terbuka, setelah 4-7 hari kalau tidak ada tanda-tanda infeksi baru dijahit, dengan indikasi sama sepert yang ditemukan dalam penyembuhan luka primer tertunda.
KOMPLIKASI LUKA
Penyulit dini :
- Hematoma : terjadi akibat hemostasis yang kurang baik. Hematoma yang besar atau mengganggu sebaiknya dibuka lalu dikeluarkan. Hematoma yang meluas perlu pembedahan ulang untuk hentikan perdarahan.
- Seroma : penumpukan cairan luka. Kalau terlalu besar atau mengganggu dapat dilakukan punksi.
- Infeksi : terjadi akibat penanganan luka yang tidak betul. Terjadi penanahan pada luka umumnya oleh kuman-kuman stafilokokus dan streptokokus. Merupakan salah satu penyebab luka terbuka kembali = dehiscentie. Luka dengan infeksi sebainya jahitan dibuka agar nanah dapat keluar, lalu dirawat terbuka.
Penyulit lanjut :
- Keloid dan jaringan parut hipertrofik. Terjadi akibat reaksi serat kolagen yang berlebihan dalam penyembuhan luka.
- Kontraktur jaringan parut luka. Terjadi pengerutan yan ghebat dari jaringan parut yang dapat mengakibatkan cacat berat / gangguan gerakan pada sendi misalnya pada luka bakar.
Perbedaan antara keloid dan parut hipertrofik :
| Keloid | Parut Hipertrofik | |
| Permulaan | Mungkin timbul kemudian, setelah beberapa bulan, atau satu-dua minggu | TImbul dalam waktu beberapa minggu |
| Invasi | Meluas ke daerah kerusakan epitel | Terbatas pada bekas kerusakan |
| Penyembuhan | Tidak ada regresi | Hilang sendiri |
| Predileksi | Sternum, bahu, pipi, telinga, pinggang | Dapat timbul di mana pun |
| Ras / bangsa | Terutama ras kulit gelap atau hitam | Lebih banyak pada bangsa kulit putih |
| Luka bakar | Mungkin | Sering |
| Gatal | Jarang hebat | Biasanya sangat menganggu |
Sebagai penutup artikel ini, telah ditemukan hal-hal yang berhubungan dengan luka dan proses penyembuhannya serta keadaan-keadaan yang mempengaruhi penyembuhan, demikian pula cara penanganannya. Diharapkan dengan dasar pengetahuan ini maka luka-luka dapat ditangani dengan baik dan benar, dengan selalu bertolak dari keyakinan bahwa : “The is no antibiotic can substitute a good surgery”.